各有關單位:
為了保護醫療器械臨床試驗受試者安全,規范臨床試驗審批工作,保證醫療器械安全性、有效性和可及性,加快產品上市,我中心對《需要進行臨床試驗審批的第三類醫療器械目錄》進行調整,形成2019年修訂版(征求意見稿)(附件1),即日起在網上公開征求意見。
衷心希望相關領域的專家、學者和從業人員提出意見和建議。如有意見或建議,請填寫反饋意見表(附件2),并將該表以電子郵件形式于2020年1月31日前反饋至我中心。
聯系人:李錚,閔玥
電 話:010-86452825,010-86452806
電子郵箱:lizheng@cmde.org.cn minyue@cmde.org.cn
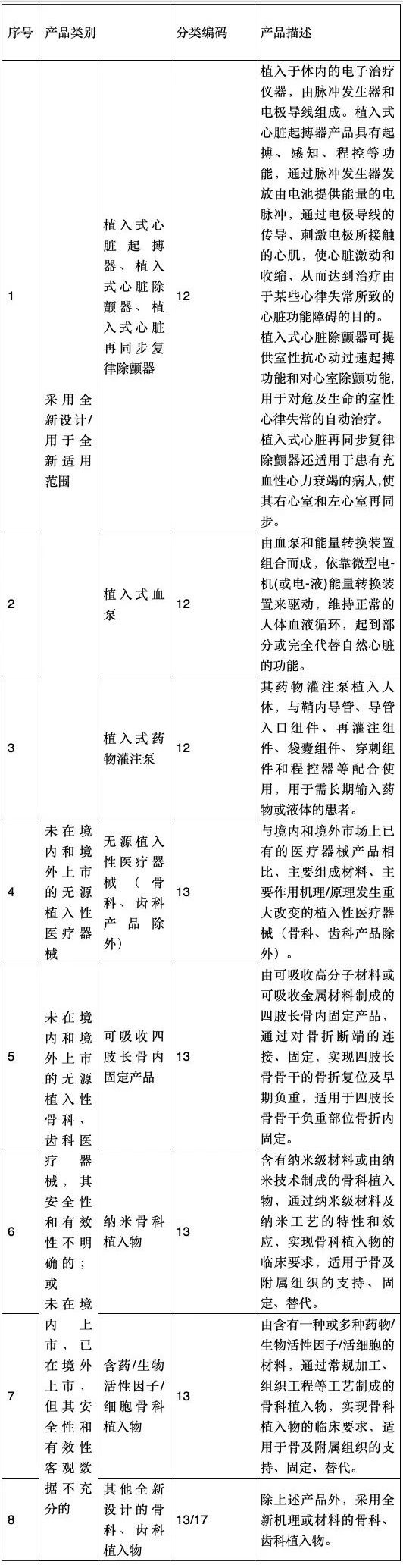
附件:1. 需要進行臨床試驗審批的第三類醫療器械目錄(2019年修訂版)(征求意見稿)(下載)
2. 反饋意見表(下載)
國家藥品監督管理局
醫療器械技術審評中心
2019年12月23日
附件1: